什麽是真實世界研究? 與随機對照研究、單病例随機對照試驗等,RWR 的區(qū)别是什麽呢(ne)?RWR又有哪些分(fēn)類呢(ne)?
人類醫(yī)學(xué)史上第一個臨床研究是JamesLind對檸檬酸治療壞血的研究,而第一個文(wén)獻報道的随機對照試驗(RCT)是有現代醫(yī)學(xué)随機對照試驗之父Austin Bradford Hill的“四環素治療肺結核”的研究。長(cháng)久以來,RCT被醫(yī)學(xué)界認為(wèi)是“理(lǐ)性療法(rationaltherapeutics)”,但RCT在實際臨床研究中存在真實性差、外推困難等問題逐漸被研究者重視。在這樣的背景下,RWR愈發獲得研究者的關注。


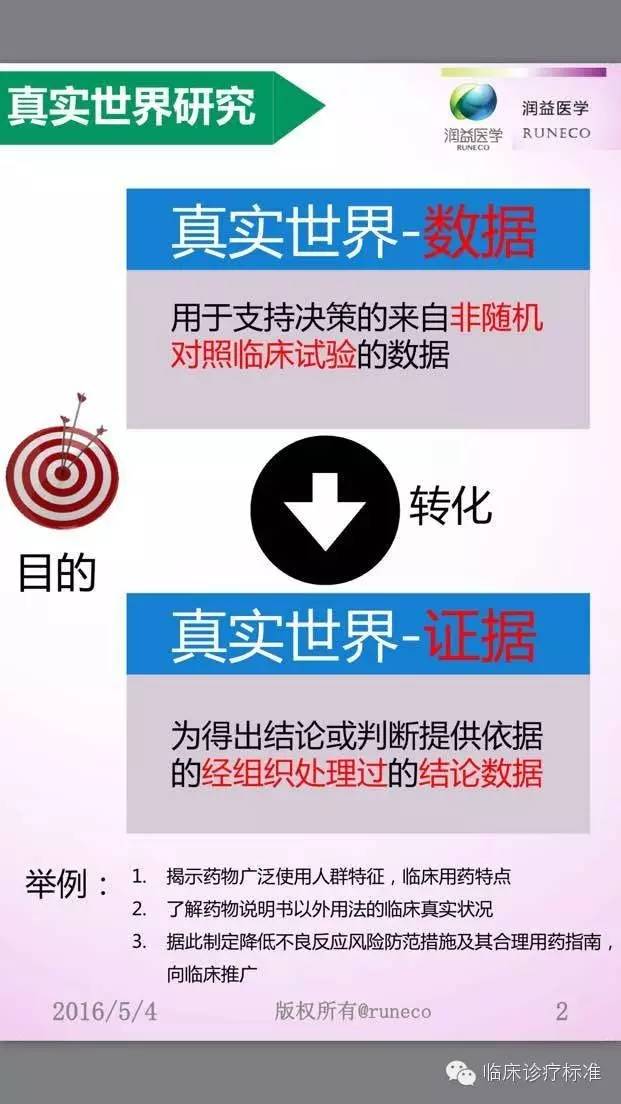
RWR起源于實用(yòng)性臨床試驗,最早應用(yòng)于藥物(wù)流行病學(xué)範圍。指在較大的樣本量(覆蓋具有代表性的更廣大受試人群)的基礎上,在真實醫(yī)療過程中,根據患者的實際病情和意願非随機選擇治療措施,開展長(cháng)期評價,并注重有意義的結局治療,在廣泛真實醫(yī)療過程中評價幹預措施的外部有效性和安(ān)全性。
RWR涵蓋的範圍較RCT更廣,除治療性研究之外,還可(kě)用(yòng)于診斷、預後病因等方面的研究。RWR的目的旨在獲得更符合臨床實際的證據,使研究結果更易轉化到臨床實踐中。與RCT相比,RWR涵蓋的範圍更廣,除治療性研究之外,還可(kě)用(yòng)于診斷、預後病因等方面的研究。 RCT所獲得的是試驗性數據,RWR所獲得的是真實數據。RCT需要回答(dá)的問題是“是否有效和安(ān)全”;RWR所回答(dá)的問題是“能(néng)否有效作(zuò)為(wèi)醫(yī)療手段”。
表1 真實世界研究與随機對照研究對比
真實世界研究(RWR) | 随機對照研究(RCT) | |
目标 | 效果研究 | 效力研究 |
時間 | 長(cháng) | 短 |
時間及方案設計 | 根據不同研究目标和内容選擇設計方案 | 試驗性方法為(wèi)主,類試驗為(wèi)輔 |
質(zhì)量控制手段 | 非随機、開放性、不使用(yòng)安(ān)慰劑的非盲試驗 | 随機分(fēn)配、盲法、标準化治療,可(kě)使用(yòng)安(ān)慰劑 |
納入和排除标準 | 較寬泛納入标準和較少的排除标準 | 嚴格的納入和排除标準 |
樣本量和代表性 | 樣本量偏小(xiǎo)則産生偏差,樣本量為(wèi)考察結果真實性的重要指标 | |
幹預 | 真實治療 | 标準化治療 |
結局測量指标 | 多(duō)采用(yòng)有廣泛臨床意義的指标:病死率、複發率、傷殘程度、生活質(zhì)量 | 多(duō)以一個或者一些特定病症或體(tǐ)征為(wèi)評價目标 |
數據采集、管理(lǐ)及統計分(fēn)析方法 | 二者都強調應嚴格控制數據采集、管理(lǐ)和分(fēn)析過程,所采用(yòng)的統計學(xué)方法學(xué)方法基本相同,如卡方檢驗、Fisher檢驗、log-rank檢驗、ROC曲線(xiàn)、Kaplan-Meier生存曲線(xiàn); | |
倫理(lǐ) | 受試者不會接受沒有任何效能(néng)的治療,更易滿足倫理(lǐ)學(xué)要求,不存在幹預等問題,故倫理(lǐ)學(xué)原則不會對研究時間、樣本量等因素産竽制約 | 受試者損害最小(xiǎo)化原則,為(wèi)避免過多(duō)的受試者接受可(kě)能(néng)療效較差的治療或發生不良反應,充分(fēn)保證受試者的權益,倫理(lǐ)學(xué)要求在進行RCT前計算樣本量,确定具有檢驗效能(néng)和得出良好可(kě)信度估計值的最小(xiǎo)樣本量 |
局限性 | 樣本量巨大,成本相對昂貴,數據處理(lǐ)難 | 外推性較差 |
表2 真實世界研究與單病例随機對照試驗比較
真實世界研究 | 随機對照試驗 | 單病例随機對照試驗 | |
樣本量 | 大 | 根據試驗設計 | 最少 |
随機對象 | 不随機 | 受試者 | 幹預措施 |
成本 | 昂貴 | 低 | 低 |
那麽RWR都包括哪些類型呢(ne)?RWR包括臨床效果研究,經濟效益研究、流行病學(xué)研究以及患者回饋調查。
①臨床效果研究 (觀察代表臨床效果的醫(yī)療指征),這種研究可(kě)以觀察多(duō)個臨床介入手段的實際效果,也可(kě)以觀察多(duō)個時間段的變化,多(duō)個地區(qū)之間的區(qū)别,以及在某種設定條件下的實際臨床效果;
②經濟效益研究(評估為(wèi)達到相同程度臨床效果所需要的資源),這種研究考量的是一個醫(yī)療手段(例如新(xīn)藥、手術方法、診斷方法等)對管理(lǐ)某病種的常規預算所産生的影響(budget impact),這種影響可(kě)以由資源節省或資源利用(yòng)等概念來顯示;
③流行病學(xué)研究 (觀察在某種條件下的原發病發病率,并發症發病率,發病或病情蔓延影響因子等);
④患者回饋調查研究(了解患者對某些治療手段的直感反應,包括症狀效果、副作(zuò)用(yòng)、便利性、生活質(zhì)量指數等),在一定規範條件下執行的患者回饋研究(patient reported outcomes)結果可(kě)以經包括美國(guó)食品與藥物(wù)管理(lǐ)局這樣的藥物(wù)審批機構認可(kě),列為(wèi)新(xīn)藥的特征之一。
↓↓↓ 下面分(fēn)享 潤益醫(yī)學(xué) 制作(zuò)的關于真實研究的珍貴材料
法邁生醫(yī)學(xué)參與全球首個抗腫瘤藥(艾迪注射液)10萬例真實世界臨床研究
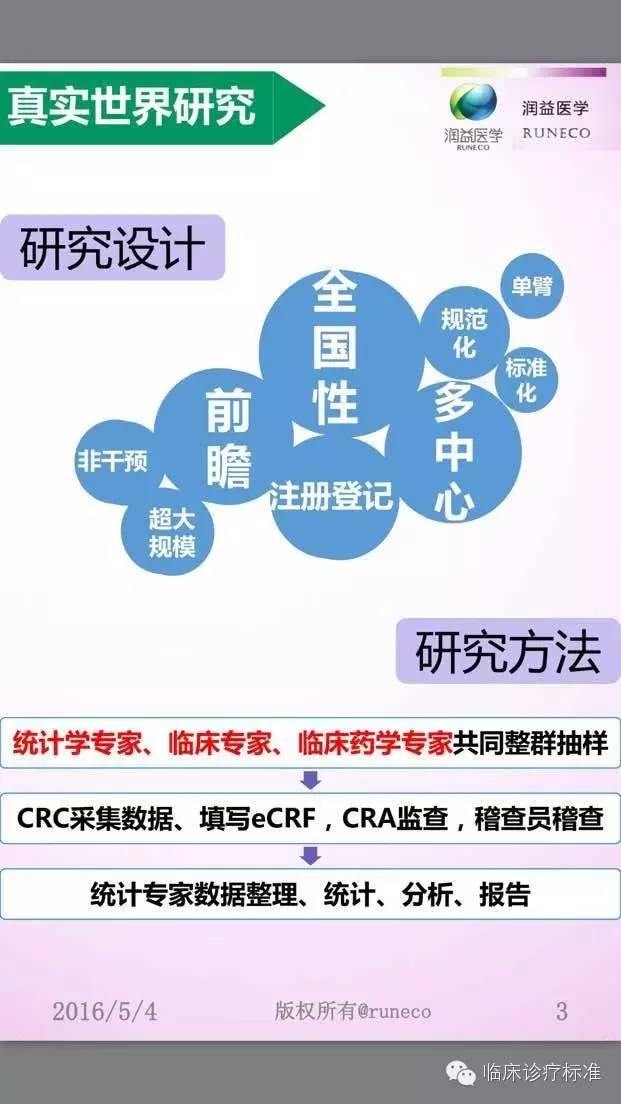
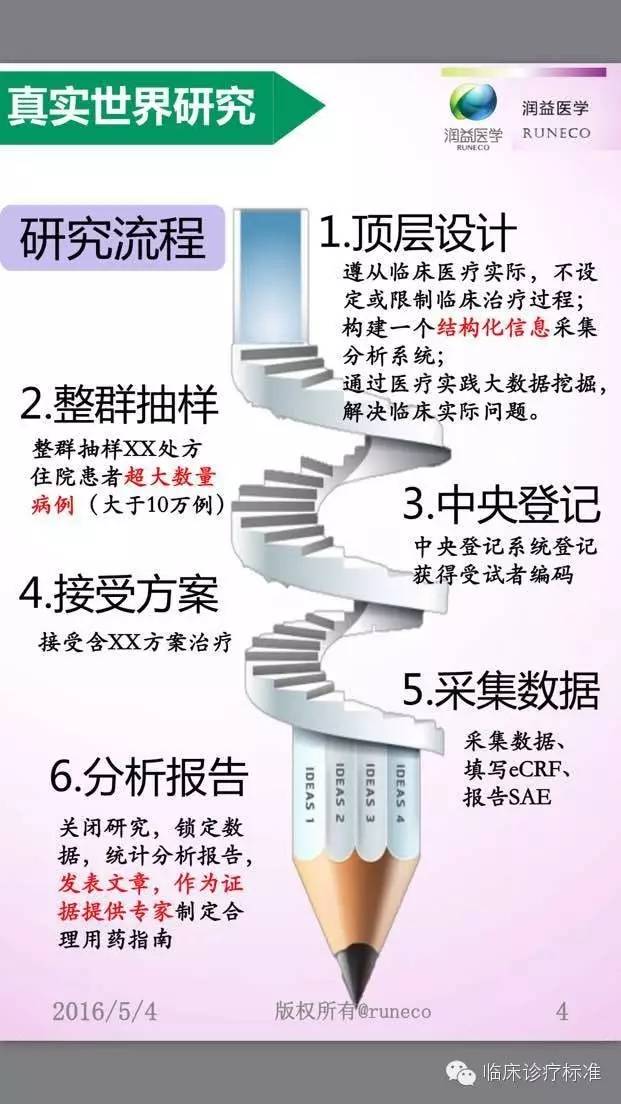
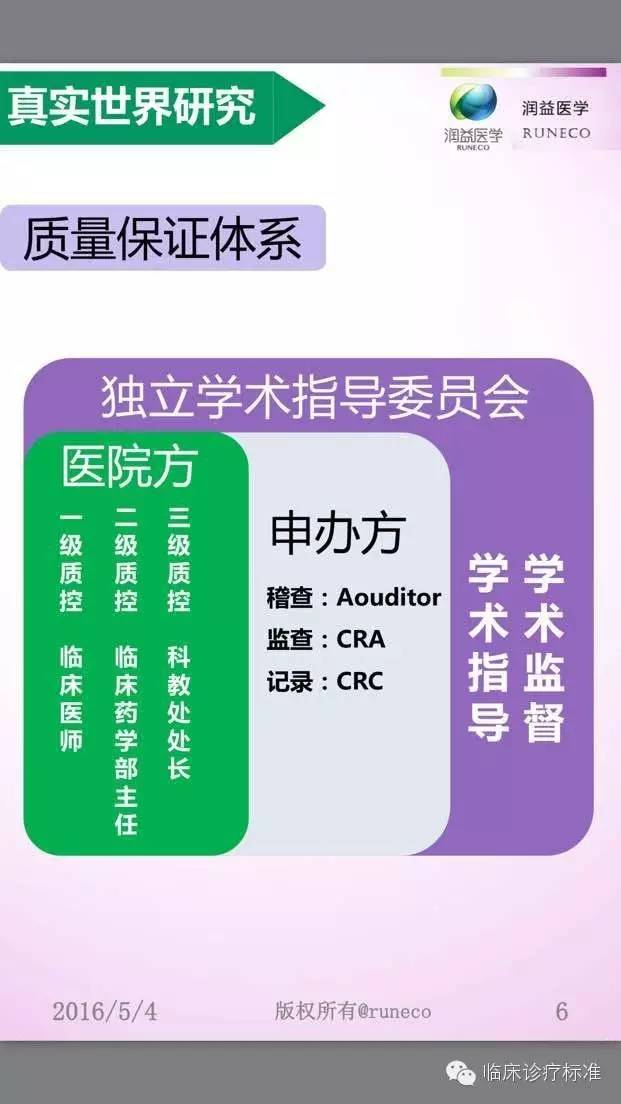
江蘇法邁生醫(yī)學(xué)科(kē)技(jì )有限公司與貴州益佰制藥股份有限公司2016年3月達成戰略合作(zuò),共同開展10萬例艾迪注射液上市後安(ān)全性再評價真實世界的研究。法邁生醫(yī)學(xué)承擔該研究中的整群抽樣、受試者注冊登記、數據采集、數據管理(lǐ)、基本統計分(fēn)析、撰寫總結報告等工作(zuò)。